 Delegación Presidencial Provincial de
Delegación Presidencial Provincial de Chacabuco

Instituto de Salud Pública amplía vacunación a niños desde los 5 años para vacuna Pfizer
La vacuna que ya ha sido aprobada por la FDA, la EMA y otras agencias internacionales, en esta misma población, se convierte en una alternativa adicional a la vacuna de Sinovac, autorizada en a niños desde los tres años, el 30 de noviembre pasado.
El Comité de Expertos de Evaluación de Vacunas del Instituto de Salud Pública (ISP), recomendó la aprobación de la solicitud de Pfizer Chile para la ampliación del rango etario en menores desde los 5 años de edad. La vacuna que ya ha sido aprobada por la FDA, la EMA y otras agencias internacionales, en esta misma población, se convierte en una alternativa adicional a la vacuna de Sinovac, autorizada en a niños desde los tres años, el 30 de noviembre pasado.
Para llegar a esta decisión, el Comité de Expertos analizó los antecedentes de los estudios clínicos fase 1, 2 y 3, que incluyeron 2.700 niños cuyas edades se encuentran dentro del nuevo rango etario.
“Ahora tenemos dos vacunas disponibles para niños lo que permite una mayor cobertura, porque en el caso hipotético de algún desabastecimiento se tiene más de una alternativa de vacunas que han demostrado ser eficaces. Además, esta vacuna cuenta con una nueva formulación aprobada hoy para niños desde los cinco años, la cual demostró tener un 90,7% de eficacia”, señaló el Director (s) del ISP, Q.F. Heriberto García.
Asimismo, García aclaró que la nueva formulación presentada por Pfizer corresponde a una modificación del componente estabilizador de PH (buffer) de la vacuna que permite mayor duración tras salir de la cadena de frío. “El producto tiene una estabilidad a temperatura ambiente de 12 horas en vez de las 6 horas que tenía la formulación anterior, lo que facilita el acceso a la vacuna sobre todo en lugares donde es más complejo mantener la cadena de frío”, señaló el Director del ISP.
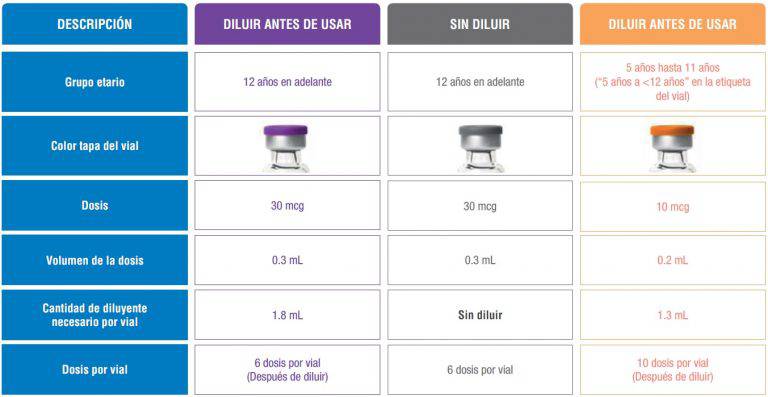
Cabe señalar que el laboratorio Pfizer Chile presentó el 11 de noviembre, la solicitud aprobada el día de hoy, y que esta nueva fórmula aplica tanto para la dosis en personas desde los 12 años (30 µg), como para la dosis para niños desde los 5 años (10 µg). Además, esta presentación contempla un nuevo rotulado gráfico de la vacuna, con distintivos de colores para reconocer las dosis para niños.
El vial de color púrpura o morado, es para los mayores de 12 años, que corresponde a la vacuna autorizada el 16 de diciembre del año 2020 donde hay que diluir la dosis de 30 microgramos. La nueva formulación de color gris, es para los mayores de 12 años donde se mantiene la cantidad de la dosis, sin embargo, la indicación muestra que la dosis no se debe diluir. Por último, la formulación de color naranja es para los niños de 5 a 11 años donde sí hay que diluir la dosis de 1,3 ml.
Farmacovigilancia
En relación a la información de seguridad en niños de 5 a 11 años en el estudio Fase 2 y 3, el Centro Nacional de Farmacovigilancia del ISP consideró que la evidencia ha contribuido a demostrar que la vacuna Pfizer presenta un buen perfil de seguridad en esta población, que se caracteriza principalmente por eventos adversos leves a moderados que son esperables y no difieren de lo que se conoce para la vacunación en general.
Volver
















